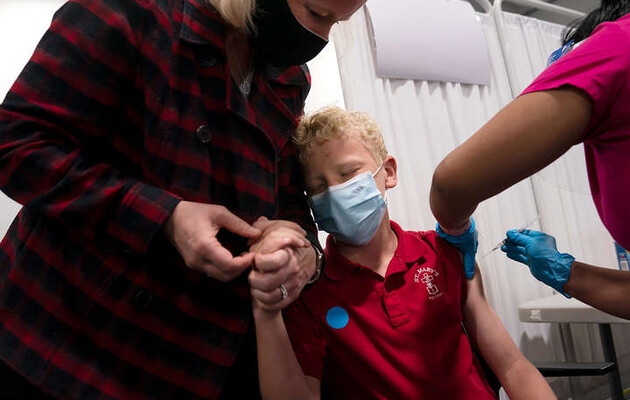
Moderna подала заявку в регулирующий орган Европейского союза в области медицины для утверждения своей вакцины против Covid-19 для детей в возрасте от шести до 11 лет, сообщила во вторник американская биотехнологическая компания.
Дозировка для двух инъекций, вводимых с интервалом в четыре недели, была скорректирована до 50 микрограммов по сравнению со 100 микрограммами для реципиентов инъекций в более старших возрастных группах.
«Мы рады объявить о представлении этого варианта в EMA», - говорится в заявлении Европейского агентства по лекарственным средствам, исполнительного директора Moderna Стефана Банселя, передает AFP.
«Это наша первая заявка на использование нашей вакцины в этой возрастной группе».
Moderna в настоящее время одобрена для людей от 12 лет и старше в Европе.
Но несколько стран, в том числе Франция в понедельник, посоветовали не использовать ее людям моложе определенного возраста (30 лет во Франции) из-за опасений по поводу риска миокардита или воспаления сердечной мышцы.
Редкий побочный эффект был обнаружен у подростков и молодых людей, особенно у мужчин.
В конце прошлого месяца Moderna сообщила о положительных результатах своих клинических испытаний для детей в возрасте от 6 до 11 лет, при этом вакцина вызвала сильный иммунный ответ с обнаруженными «устойчивыми» уровнями нейтрализующих антител.
EMA также рассматривает данные компании Pfizer, которая подала заявку на европейское одобрение собственной вакцины для детей в возрасте от 5 до 11 лет. Этот обзор может быть завершен в декабре, сообщило агентство на прошлой неделе.
Вакцина Pfizer уже лицензирована для использования у маленьких детей в Соединенных Штатах, где вакцина Moderna одобрена только для детей от 18 лет и старше.
В конце октября Moderna объявила, что отложит подачу заявки на одобрение в США для детей от 6 до 11 лет, пока FDA не завершит рассмотрение для возрастной группы 12-17 лет, которое может занять до января.
Как сообщалось, Коста-Рика первой в мире ввела обязательную вакцинацию детей от COVID-19.

















 Войти с помощью Google
Войти с помощью Google