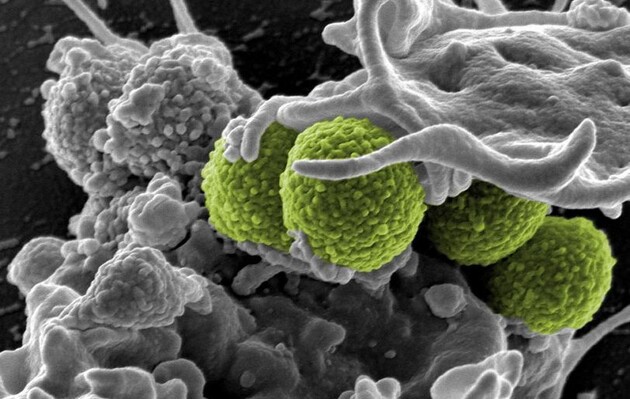
Вчені стверджують, що розробили новий тип антибіотиків для боротьби із бактеріями, які є стійкими до більшості сучасних антибіотиків і вбивають великий відсоток людей з інвазивною інфекцією, пише CNN.
Згідно з даними Центру з контролю та профілактики захворювань США, бактерія Acinetobacter baumannii може викликати серйозні інфекції в легенях, сечовивідних шляхах і крові. Вона є стійкою до класу антибіотиків широкого спектру дії, які називаються карбапенемами.
У 2017 році Acinetobacter baumannii, також відомий як CRAB, був першим у списку Всесвітньої організації охорони здоров’я стійких до антибіотиків патогенів. Того року у Сполучених Штатах бактерії спричинили приблизно 8500 інфекцій у госпіталізованих пацієнтів і 700 смертей.
На CRAB припадає близько 2% інфекцій, виявлених у лікарнях США. Він більш поширений в Азії та на Близькому Сході та викликає до 20% інфекцій у відділеннях інтенсивної терапії в усьому світі.
Бактерії поширені у таких закладах, як лікарні та будинки для людей похилого віку. Люди з найвищим ризиком інфікування – це ті, хто має катетер, хто знаходиться на апараті штучної вентиляції легень або хто має відкриті рани після операції.
Патоген настільки важко усунути, що Управління з контролю за продуктами й ліками США понад 50 років не схвалювало новий клас антибіотиків для його лікування, відзначають автори у своєму дослідженні, опублікованому в середу в журналі Nature.
Однак дослідники з Гарвардського університету та швейцарської медичної компанії Hoffmann-La Roche стверджують, що новий антибіотик, зосурабалпін, може ефективно вбивати Acinetobacter baumannii.
«Зосурабалпін» належить до власного хімічного класу та має унікальний метод дії. Це новий підхід як щодо самої сполуки, так і щодо механізму, за допомогою якого вона вбиває бактерії», — переконує доктор Кеннет Бредлі, один із дослідників, керівник глобального відділу виявлення інфекційних захворювань Roche Pharma Research and Early Development.
Acinetobacter baumannii є грамнегативною бактерією, тобто вона захищена внутрішньою та зовнішньою мембранами, що ускладнює лікування. Метою дослідження було ідентифікувати та налаштувати молекулу, яка могла б перетинати подвійні мембрани та вбивати бактерії.
«Ці дві мембрани створюють дуже потужний бар’єр для проникнення молекул, таких як антибіотики», — сказав Бредлі.
Дослідники почали розробку зосурабалпіну, вивчивши близько 45 тисяч невеликих молекул антибіотиків, які називаються прив’язаними макроциклічними пептидами, і виявивши ті з них, які можуть пригнічувати ріст різних типів бактерій. Після багатьох років покращення ефективності та безпеки меншої кількості сполук дослідники зупинилися на одній модифікованій молекулі.
Зосурабалпін пригнічує ріст Acinetobacter baumannii, перешкоджаючи руху великих молекул, які називаються ліпополісахаридами, до зовнішньої мембрани, де вони необхідні для підтримки її цілісності. Це призводить до того, що молекули накопичуються всередині бактеріальної клітини і стають настільки токсичними, що сама клітина гине.
За даними дослідження, зосурабалпін був ефективним проти більш ніж 100 протестованих клінічних зразків CRAB.
За словами дослідників, антибіотик значно знизив рівень бактерій у мишей із пневмонією, спричиненою CRAB. Це також запобігло смерті мишей із викликаним бактеріями сепсисом.
«Виявлення ліків, спрямованих на шкідливі грамнегативні бактерії, є давньою проблемою через труднощі в тому, щоб молекули перетнули мембрани бактерій, щоб досягти цілей у цитоплазмі. Успішні сполуки зазвичай повинні мати певну комбінацію хімічних характеристик», — пишуть дослідники.
За словами авторів дослідження, зосурабалпін зараз проходить першу фазу клінічних випробувань для оцінки безпеки, переносимості та фармакології молекули у людей.
Проте загроза громадському здоров’ю, пов’язана із резистентністю до протимікробних препаратів, залишається величезною в усьому світі через відсутність ефективних методів лікування, вважає доктор Майкл Лобріц, глобальний керівник відділу інфекційних захворювань Roche Pharma Research and Early Development, який також брав участь у дослідженні.
Стійкість до антимікробних препаратів виникає, коли такі мікроби, як бактерії та гриби, розвиваються настільки, що здатні пережити контакти з препаратами, призначеними для їх знищення.
Відповідно до опублікованого в Lancet аналізу 2022 року, у 2019 році близько 1,3 мільйона людей в усьому світі померли безпосередньо від стійкості до антимікробних препаратів. Для порівняння, ВІЛ/СНІД і малярія того ж року спричинили 860 тисяч і 640 тисяч смертей відповідно.
За останні десятиліття було розроблено низку антибіотиків для лікування грампозитивних інфекцій, які зазвичай менш шкідливі та менш стійкі до антибіотиків, ніж грамнегативні бактерії, сказав Лобріц.
«Грамнегативні бактерії упродовж тривалого часу накопичували резистентність до багатьох антибіотиків першого ряду, яким ми віддаємо перевагу», — сказав він, і зосурабалпін нараз є єдиним антибіотиком проти небезпечного патогену.
Незважаючи на те, що попереду додаткові дослідження, а до клінічного використання зосурабалпіну ще багато років, це надзвичайно багатообіцяюча розробка, вважає доктор Сесар де ла Фуенте, президентський помічник професора в Університеті Пенсільванії.
«Я думаю, що з академічної точки зору, це захоплююче побачити новий тип молекули, яка вбиває бактерії іншим способом. Нам, звичайно, потрібні нові нестандартні способи мислення про відкриття антибіотиків, і я думаю, що це хороший тому приклад», — наголосив він.
Єдиним недоліком, відзначають дослідники, є те, що модифікована молекула працюватиме лише проти конкретних бактерій, для знищення яких вона призначена.
Проте де ла Фуенте каже, що сам метод модифікації молекул для націлювання на конкретні бактерії може бути кращим і для нашого загального здоров’я, адже більшість антибіотиків широкого спектру дії вбивають корисні бактерії в нашому кишечнику та на нашій шкірі.
«Протягом десятиліть ми були одержимі створенням або відкриттям антибіотиків широкого спектру дії, які вбивають усе. Чому б не спробувати створити конкретні, більш цілеспрямовані антибіотики, спрямовані лише на патоген, який викликає інфекцію, а не на всі інші речі, які можуть бути корисними для нас?», — сказав він.
Чим загрожує неконтрольоване призначення і вживання антибіотиків та що із цим робити, читайте у статті Алли Котляр «Обережно, антибіотик!».
Важливо! Ця публікація заснована на останніх та актуальних наукових дослідженнях у сфері медицини та має виключно загальноінформаційний характер. Публікація не може бути підставою для встановлення будь-яких діагнозів. Якщо ви захворіли або потребуєте діагнозу, зверніться до лікаря!