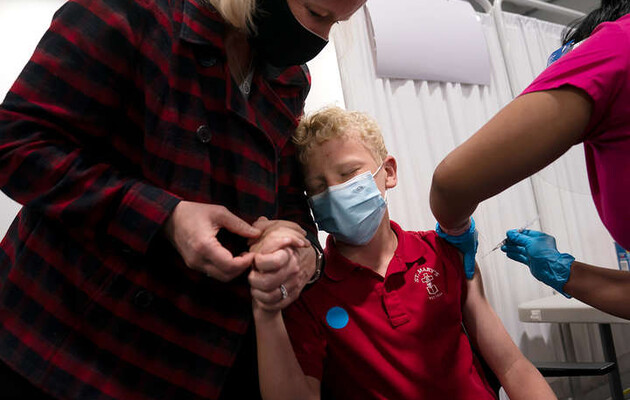
Moderna подала заявку до регулюючого органу Європейського союзу в галузі медицини для затвердження своєї вакцини проти Covid-19 для дітей віком від шести до 11 років, повідомила у вівторок американська біотехнологічна компанія.
Дозування для двох ін'єкцій, що вводяться з інтервалом у чотири тижні, було скориговано до 50 мікрограмів порівняно зі 100 мікрограмами для реципієнтів ін'єкцій у старших вікових групах.
"Ми раді оголосити про подання цього варіанту в EMA", - йдеться в заяві Європейського агентства з лікарських засобів, виконавчого директора Moderna Стефана Банселя, передає AFP.
«Це наша перша заявка на використання нашої вакцини у цій віковій групі».
Moderna в даний час схвалена для людей віком від 12 років і старших у Європі.
Але кілька країн, у тому числі Франція в понеділок, порадили не використовувати її людям молодше за певний вік (30 років у Франції) через побоювання з приводу ризику міокардиту або запалення серцевого м'яза.
Рідкісний побічний ефект був виявлений у підлітків і молодих людей, особливо у чоловіків.
Наприкінці минулого місяця Moderna повідомила про позитивні результати своїх клінічних випробувань для дітей віком від 6 до 11 років, при цьому вакцина викликала сильну імунну відповідь із виявленими «стійкими» рівнями антитіл.
EMA також розглядає дані компанії Pfizer, яка подала заявку на схвалення власної вакцини для дітей у віці від 5 до 11 років. Цей огляд може бути завершено у грудні, повідомило агентство минулого тижня.
Вакцина Pfizer вже ліцензована для використання у маленьких дітей у Сполучених Штатах, де вакцина Moderna схвалена лише для дітей віком від 18 років та старших.
Наприкінці жовтня Moderna оголосила, що відкладе подання заявки на схвалення в США для дітей віком від 6 до 11 років, поки FDA не завершить розгляд вікової групи 12-17 років, який може зайняти до січня.
Як повідомлялося, Коста-Ріка першою у світі запровадила обов'язкову вакцинацію дітей від COVID-19.